近日,我校药学院李洪林/陈卓/徐玉芳教授团队联合华东师范大学药学院研究团队,在cell旗下综合性学术期刊《the innovation》(if = 25.7)发表题为“design and development of novel egfr inhibitors spanning all subgroups of egfr mutations in non-small cell lung cancer”的研究论文。该研究发现atp结合域背后的保守疏水亚口袋,据此设计了泛egfr抑制剂zw-49,可强效抑制所有egfr突变亚型(经典型、t790m 型、ex20ins、pacc),且安全性优异,目前已完成ⅰ期临床试验(ctr20212743),为nsclc精准治疗开辟新路径。
egfr突变的异质性是传统药物难以全面覆盖的核心原因,最新研究改变基于外显子的分类方式,基于临床药物敏感型将egfr突变分为经典型、t790m型、ex20ins型和pacc型四大亚型,不同亚型的结构差异导致药物结合效率悬殊。研究团队通过对内部化合物库的多重筛选和结构叠加分析突破性发现,所有egfr突变亚型的atp 结合域背后,均存在一个由αc螺旋、β3和β5折叠形成的保守疏水亚口袋,该亚口袋不被atp占据且结构稳定。对该亚口袋进行自由能景观分析,破解高亲和力残基,成为设计泛egfr抑制剂的关键位点。基于此,团队以先导化合物3x为基础,引入取代基衍生优化得到zw-49,使其能够同时占据传统atp口袋与保守亚口袋,既增强了与所有突变体的亲和力,又规避了p环压缩带来的空间位阻,从机制上解决了耐药难题。
研究团队证实,候选药物zw-49对14种临床相关egfr/her2突变的抑制活性达纳摩尔级(ic₅₀=0.03-0.41 nm),对经典型、ex20ins型、pacc型等突变的抑制效果优异,且对野生型egfr 具有6.6倍的选择性,可有效降低皮疹、腹泻等副作用风险。借助分子动力学模拟,团队进一步明确zw-49与egfr突变体的结合自由能达-72.78 kcal/mol,构象稳定性远优于其他衍生物。在h1975、baf3(g719a)、baf3(d770_n771insnpg)等4种肺癌异种移植模型中,zw-49口服给药展现出强大的抗肿瘤效果,肿瘤生长抑制率最高达120.27%,且未引起小鼠明显体重下降,安全性优势显著。
为提升zw-49的药代动力学性能,团队通过自主研发的代谢预测算法锁定主要代谢位点,设计并合成了氘代衍生物zw-49a-e。其中zw-49b和zw-49d的口服生物利用度提升2.4-3.0倍,血浆暴露量增加约10倍,同时保留了原药对所有egfr突变亚型的强效抑制活性。
综上,该研究首次揭示保守疏水亚口袋作为泛egfr抑制剂的设计靶点,成功开发出兼具强效性、高选择性和优异药代动力学性能的zw-49b。该药物不仅破解了egfr突变异质性带来的治疗困境,更建立了“结构导向设计 代谢优化”的泛抑制剂开发范式,为nsclc精准治疗提供了全新策略。目前zw-49和zw-49b的相关研究仍在推进,有望为ex20ins、pacc等难治性突变患者带来新的治疗希望。
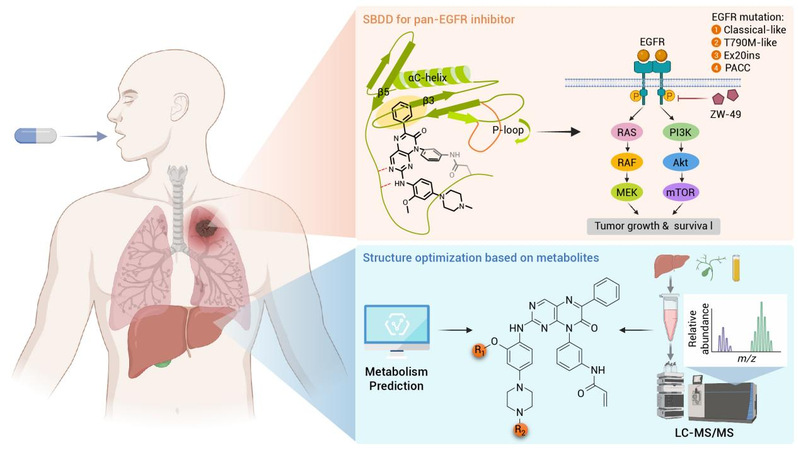
图1:泛egfr抑制剂研发策略
华东理工大学药学院博士生王操林,岑逸婷和张满湛为本论文的共同第一作者。华东理工大学药学院徐玉芳教授、陈卓副研究员和华东理工大学/华东师范大学药学院李洪林教授为该论文的通讯作者。研究工作得到国家自然科学基金、国家重点研发计划和中央高校基础科研业务费专项资金等项目资助。
原文链接:https://www.cell.com/the-innovation/fulltext/s2666-6758(26)00060-3